有害事象/副作用発現率、発現時期及び適正使用の目安
エスワンタイホウ単独療法〈胃癌術後補助療法〉
主な有害事象発現率(n=517)
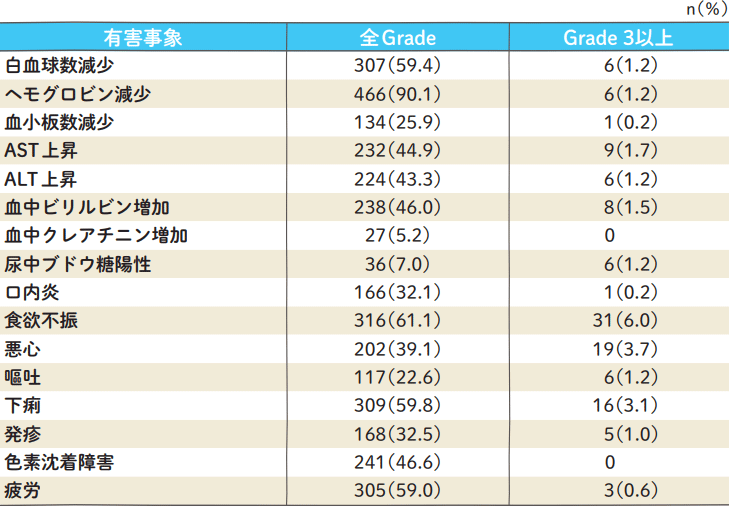
Grade分類は、NCI-CTC ver.2.0で集計
ACTS-GC試験統括報告書より作成
適正使用の目安
ULN:(施設)基準値上限
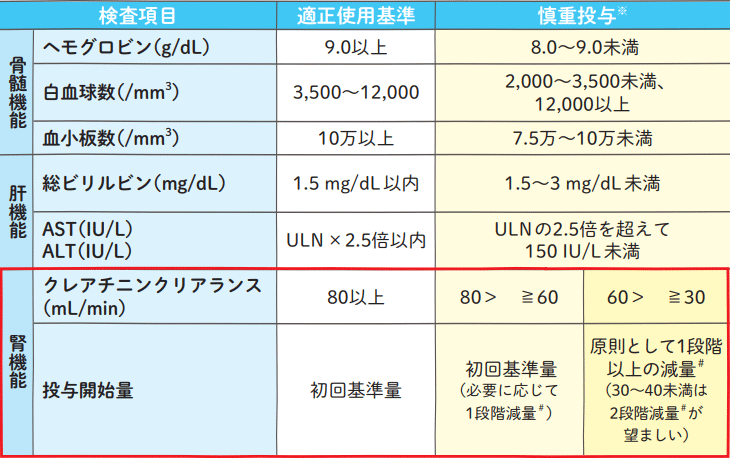

投与開始量は、クレアチニンクリアランス(実測値あるいは推定値)だけで定まるものではなく、患者の状態によっては80 mL/min以上の症例であっても減量が必要な場合もある。
※:適正使用基準に回復するまで投与延期することが望ましく、本剤の投与を必要とする場合には頻回に検査し、慎重に観察しながら投与する。
#:先発品(ティーエスワン)の承認治験においては、最低投与量は40 mg/ 回としていた。
注:重篤な骨髄抑制のある患者、重篤な腎障害のある患者、重篤な肝障害のある患者には投与しないこと。
休薬・減量・再開の目安
ULN:(施設)基準値上限 ( ):目安となる検査値の絶対値 TPN:非経口栄養
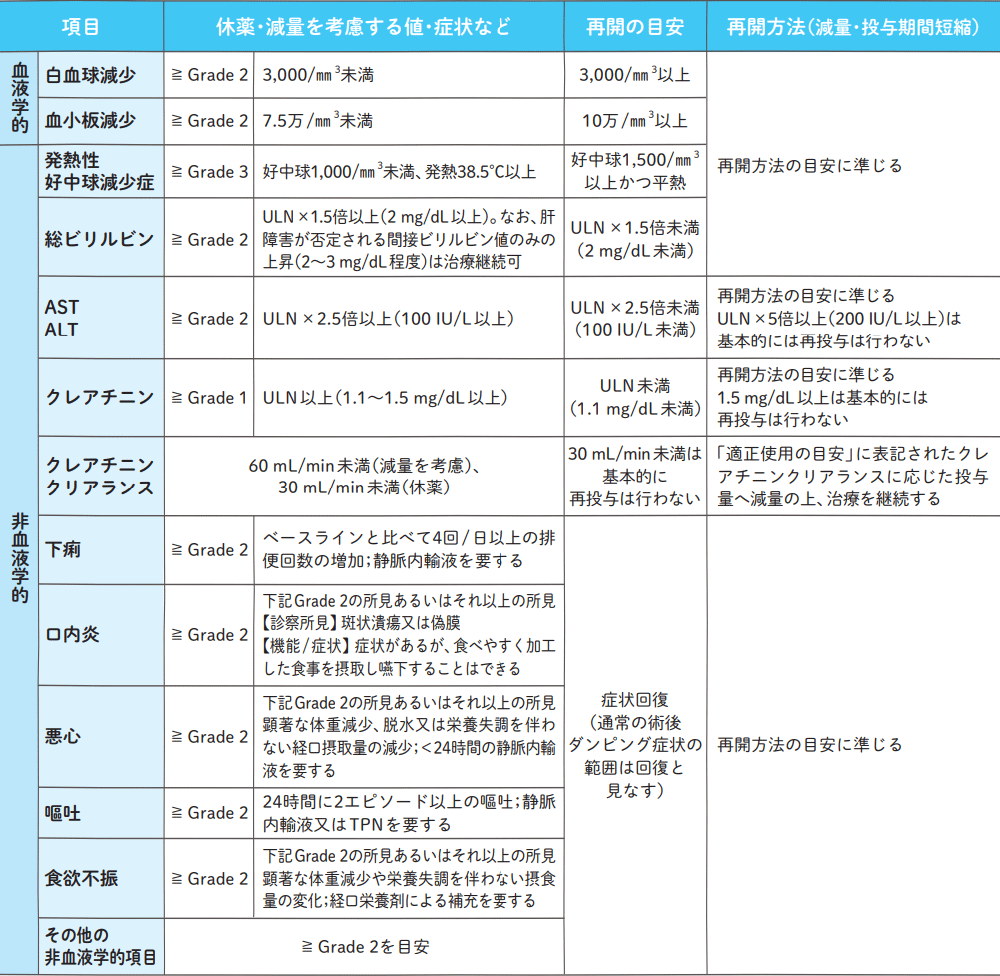
再開方法の目安

注1:休薬を考慮する値・目安のGradeはCTCAE v3.0をベースにエスワンタイホウ適正使用の目安を基に一部変更を加えて作成。
注2:休薬・減量・再開の目安であって、絶対的なものではないため、患者の状態や発現時期などを考慮して休薬や再開を決定。
エスワンタイホウの使用にあたっては用法及び用量をご参照ください。

